یکی از شاخه های علم زیست شناسی و صد البته بیوفیزیک، علم پرتوشناسی زیستی با رادیوبیولوژی است. در این علم به چیستی پرتوهای رادیواکتیو و اثر آنها بر موجود زنده پرداخته می شود. پرتوهای آلفا، بتا، پوزیترون و گاما از مهمترین و فراوان نترین پرتوهای رادیو اکتیو هستند که در نتیجه الودگیهای رادیواکتیو و یا انفجارهای اتمی منجر به مرگ و اسیب دیدن بسیاری از موجودان و انسان می شوند
| پرتو آلفا | پرتو بتا | پرتو گاما | |
| طبیعت | هسته اتم هلیوم | الکترون | پرتوالکترومغناطیس |
| بار الکتریکی | + | - | فاقد بار الکتریکی |
| جرم | سنگین | سبک | فاقد جرم |
| سرعت | کند | سریع | سرعت معادل سرعت نور |
| قدرت یونیزاسیون | بسیار زیاد | متوسط | کم |
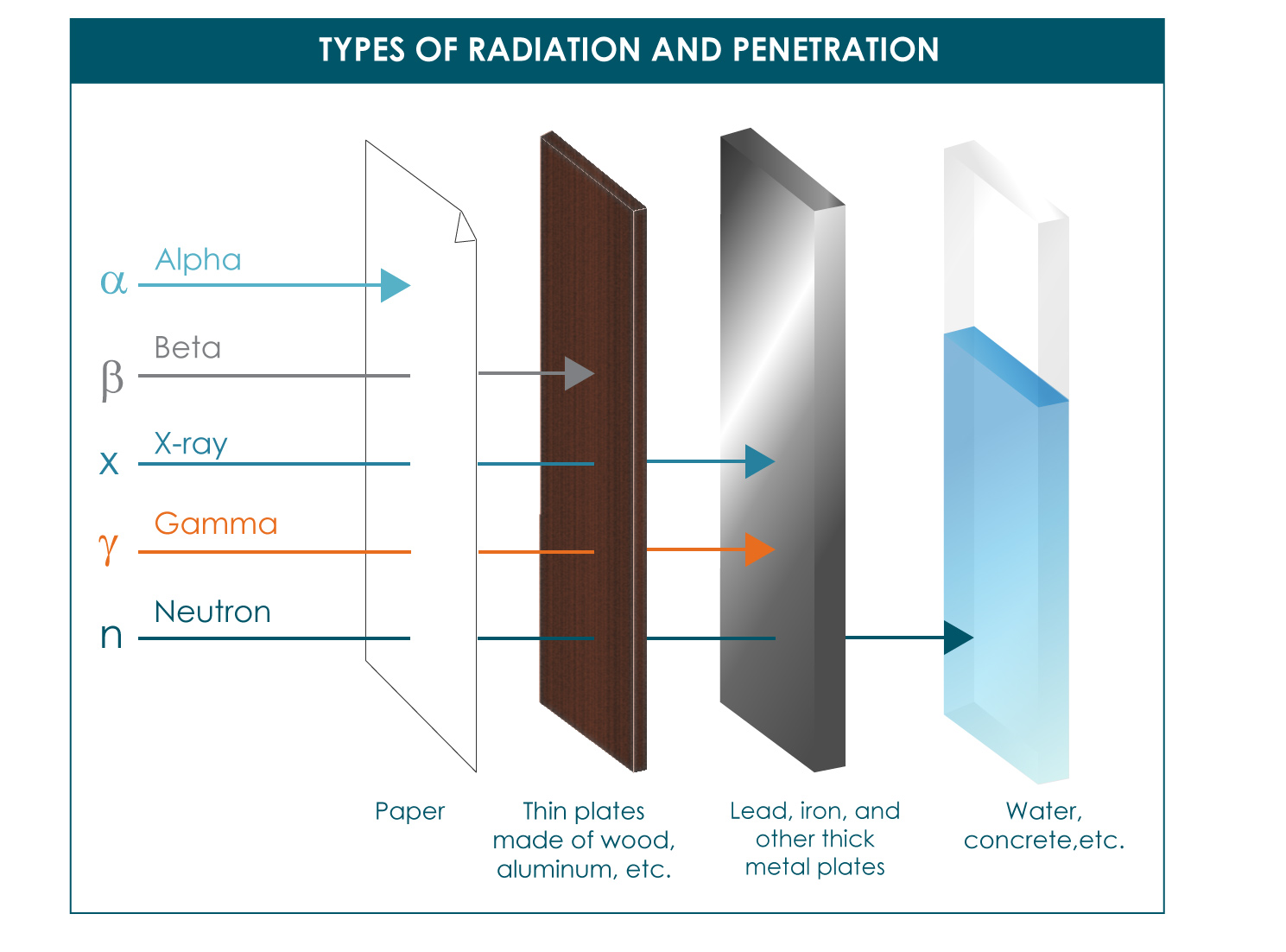
پرتوهای الفا علی رغم اینکه قدرت تخریب زیادی دارند اما قدرت نفوذ بسیار کمی دارند به صورتی حتی از لباس هم عبور نمی کنند و پوست انسان به سادگی مانع از نفوذ آن می شود. این پرتوها در صورتی خطرناکند که تنفس شوند و یا خورده شوند.
پرتوهای بتا و پوزیترون، از پوست انسان می گذرند و به راحنی واد بدن می شوند. دیوار اجری و بتونی معمولی به راحتی مانع از نفوذ این پرتوها می شوند.
پرتوهای گاما قدرت نفوذ بسیار زیتدی دارند به صورتی که تنها صفحات ضخیم سرب و دیوار های بتنی ذخیم مانع از عبور آنها می شود.
درعلم زیست شناسی سلولی پیشرفته و امروزی این سوال مطرح است که چگونه سلولهای بزرگ و پیچیده شکل گرفته و حفظ می شوند. این مساله همچنان پیچیده است که چه عاملی شکل های مختلف سلولها و اندازه آنها را تعیین می کند.
دو مکانیزم عمده و متفاوت در تولید یا کرومولکولها موثر است : Self-organization , Self-assembly . میانگین فیزیکی مولکولها در شرایط تعادل Self- assembly, equilibrium state نامیده می شود. به عبارتی دیگر self-assembly مولکولها با یکدیگر میانگین دارند تا به تعادل برسند. در حالیکه خود ساماندهی یا self-organization شامل میانکنشهای فیزیکی است که منجر به ساختارهای پایا ( steady state) می شود. برای مثال پروتئینهای ویروسها و فاژها self-assemble می شوند تا در یک حالت تعادلی به ساختارهایی پایدار و استاتیک (ثابت) برسند.درمقابل بیشتر ساختارهای سلولی (اسکلت درون سلولی،اجزاء درون هسته،اجزاء اندوکراین و .) قابلیت تحمل تغییر ماده و انرژی را دارند و بنابراین در شرایط دینامیک . steady-state هستند.
تفاوت حالت Steady – state, equitibrium
برخی از واکنشها برگشت پذیرو برخی برگشت ناپذیرند. در یک واکنش مانند تبدیل A→B در هر لحظه واکنشگر (A) به محصول (B) تبدیل می شود. در درسته ای از واکنشها که واکنشهای برگشت پذیر نامیده می شوند، واکنشگرها می توانند مجددأ از محصول تولید شوند. در حالی که واکنشهای برگشت ناپذیر هرگز محصول مجددأ به مواد اولیه تبدیل نخواهد شد. دریک واکنش برگشت پذیر، مسیر تبدیل مواد اولیه به محصول ، مسیر رفت و مسیر تبدیل محصول به مواد اولیه مسیر برگشت نامیده می شود. هنگامی که سرعت مسیر رفت و برگشت با یکدیگر برابر باشد، سیستم (واکنش)دو حالت تعادل یا eqilibrium قرار می گیرد. در این حالت با گذشت زمان مقداری ماده اولیه و محصول ثابت باقی خواهد ماند. لازم به ذکر است که در شرایط تعادل مقدار ماده اولیه و محصول وماً برابر نیست.اما در حالت پایاپا steady state ،واکنشی تقریباً به صورتA→B→C رخ می دهد که در آن A نهایتاً به B تبدیل می شود اما با تشکیل یک حد واسط به نام B . قبل از اینکه واکنش آغاز شود ، تنها A وجود دارد و B به آرامی شروع به تولید مثل می کند. با گذشت زمان از تعداد A کم شده و مقدار افزایش می یاد. اما مقدار B تقریباً ثابت باقی می ماند. این حالت ، همزمان با اینکه مقدار B زیاد شود، مقدار C نیز زیاد خواهد شد. به این ترتیب مقدار B تقریباً ثابت است. در این شرایط B در حالت Steady-state است.
به این ترتیب می توان گفت که دو حالت تعادل و پایا تفاوتهای زیر را با یکدیگر دارند:
مثالهای متنوعی از دو حالت پایا و تعادلی در سیستم های بیولوپزیک وجود دارد. برای مثال ثبات PH خون را می توان نمونه ای از حالت تعادل دانست. چرا که در خون ترکیباتی مانند کربوناتها و یا فسفاتها وجود دارد که نقش باتری داشته و محتوای [H] خون را تنظیم می کنند ، اما حفظ غلظت کربوناتها و یا فسفاتها به عهده سیستم های پایا یا Steady-state است. در یک نگاه کلی می توان گفت که حالت تعادل اغلب مربوط به مجموعه های غیرآلی است ، و مجموعه های آلی و زنده حالتهای پایایی غالبتری دارند.
برای مثال درون سلول، مواد معدنی دارای غلظت ثابتی هستند اما این ثبات منوط به جابجایی مداوم مواد از غشاء سلول است. به عنوان نمونه غلظت پتاسیم در سلولهای جانوری، از طریق انتقال فعال مواد و بر مبنای گرادیان الکتروشیمیایی آنها حفظ می شود. اما غلظت اکسیژن در فضای میان بافتی که تقریباً تعادل مقدار آن در سلول است نمونه ای از حالتهای تعادلی در سیستم های بیولوژیک است.
تفاوت Self-assmbly , Self-organization
مفهوم خودساماندهی یا self- organization عمدتاً بر پایه واکنشهای شیمیایی است که از حالت تعادلی دور هستند و این پدیده درفیزیک ، شیمی، اکولوژی و دیده می شود. در علم زیست شناسی سلولی خودساماندهی به صورت ظرفیت و پتانسیل یک ماکرومولکول یا مجموعه ای از ماکرومولکوبها و یا اندامها برای میانکنش دادن با یکدیگر و تولید یک ساختار واحد جذبه وفعال است. در یک مجموعه خودساماندهی شده ، نوع میانکنشهای بین اجزاء ویژگیها و خصوصیات مجموعه را تعیین می کند. به این ترتیب می توان به این نتیجه رسید که یک مجموعه خودساماندهی شده قابلیت انعطاف و تحمل شرایط را دارد.
یک ساختار سلولی خودساماندهی شده باید دینامیک بوده و ترکیبات آن مرتباً مبادله شوند و نیز باید قادر باشند تا ساختارهای نسبتاً پایداری بسازند. درون سلول بسیار دینامیک و پویا است. پروتئینها،محموعه های پروتئینی و ذرات روغنی و اسیدی به سرعت درون سلول حرکت می کنند. ضریب انتشار ظاهری پروتئنها بین 0.2-20 um ²s ¯ در سیتوپلاسم است. این مسأله برای پروتئینها این امکان را فراهم می کند تا فواصلی در حد چند میکرومتر را در چند ثانیه طی کنند. در این شرایط باتوجه به تعداد بالای کپی ها از هم ماکرومولکولها ، ماکرومولکولها مرتباً با یکدیگر برخورد می کنند. از طرف دیگر اندامهای سلولی ممکن است ساختارهایی بدون تغییر و غیر دینامیک به نظر برسند اما امروزه این مسأله مشخص شده است که آنها نیز در تبادل مداوم ماده و انرژی هستند.بنابراین برخلاف ظاهر آرامشان بسیار دینامیک اند. عموماً تحرک بالای پروتئینها، سرعت بالای تبادلات و نیز تولید ساختارهای پایدار از میانکشنهای گذرای بین اجزاء بیانگر وجود و حاکمیت فرآیند خودساماندهی در میان سلولها است.
نمونه هایی از خودساماندهی : اسکلت درون سلولی و هسته سلول
مفهوم خودساماندهی بنحوی در مطالعه اسکلت درون سلولی و رشته های اکتین و میکروتوبولها مشخص است. پلی مرهای اکتین و میکروتوبول ها شکل و قطبیت سلول را می سازند و یک چهارچوب درون سلولی می سازند که نقش کلیدی در تقسیم سلول دارد. هرکدام از این نقشها در بند آرایش متفاوتی از اسکلت درون سلولی است.
پلی مرهای اکتین ومیکروتوبولها ذاتاً ناپایداراند.و مرتباً از یک سر ساخته واز سر دیگر تخریب می شوند. این تغیر و تبادل مداوم زیر واحدها و میانکنش آنها با پروتئینها برای تشکیل یک اسکلت سلولی انعطاف پذیر ضروری است. خصوصیت خودساماندهی اسکلت درون سلولی میکروتوبولها به خوبی با ترکیب توبولین، موتورهای میکروتوبولی و ATP بروز می کنند. بسته به غلظت نسبی موتور و توبولین، الگوهایی ساختاری متفا وت خواهد بود.(ساختارهای تصادفی ، ستاره ای و). محصول فرآیند پلیمریزاسیون تنها تحت تأثیر غلظت مواد اولیه وسرعت واکنش بین آنها است. همانطوری که از واکنشهای خود سامانده انظار می رود، تبدیل یک حالت ارایشی به یک حالت دیگر تدریجی نبوده و به سرعت رخ می دهد.
از طرف دیگر خزیدن (crawling) فیروبلاستها توسط تغیر شکل مرتب، تقریباً تصادفی و دائم اکتین صورت می گیرد. امروزه مطالعات نشان داده اند که رشته های اکتینی که به غشاء سلول نزدیکتراند، تمایل بیشتری به رشد در جهت خزیدن دارند، تا سایر جهات ( وقتی سلول می خواهد در جهت خاصی حرکت کند، اکتینهای سطحی به آن سمت رشد می کنند). این مسأله نشان می دهد که سینتیک پلیمریزاسیون اکتین تا چه اندازه می تواند بر عملکرد دست سلول موثر باشد.
خودساماندهی نقش بزرگی نیز در تشکیل و حفظ ساختار هستک در سلولها ی داران دارد. اگرچه هستک یکی از اجزاء دائمی هسته است اما پروتئینهای موجود در آن مرتباً بین هستک و نوکلئوپلاسم مبادله می شوند. این مجموعه، مجموعه ای پایدار و ثابت از اجزائی پویا و دینامیک است. شکل ظاهری هستک مستقیماً به فعالیت آن مربوط می شود. هنگامی که فرآیند ترجمه ریبوزومی مهار می شود، هستک ناپدید می شود و یا در جریان تقسیم سلولی درمرحله M ژنهای ریبوزومی سرکوب می شوند و در نتیجه هستک ناپدید می شود. درحالی که در مرحله تلوفاز که سرکوب از ژنهای ریبوزومی برداشته می شود، هستک نیر مجدداً ظاهر می گردد. مطالعات میکروسکوپی گواه آن است که تشکیل مجدد هستک ، نتیجه فرآیندهای خود سامانده است.
بطور خلاصه می توان گفت که شرایط لازم برای خودساماندهی وجود عوامل متعدد، قواعد ساده، میانکنشهای فراوان و عدم تمرکز بریک تعامل است. همواره وجود فرآیند خودساماندهی منجر به ایجاد خصوصیات وتواناییهای جدید می شود که این ویژگیها بزرگ وعمده بوده و بر سطوح پاینتر موثراند ( تغیر در سطح بزرگ بر سطوح یاینتر و ریزتر اثرمی گذارد. سیستم با تغیر در اجزا می تواند تغیرات بزرگ را ایجاد نماید.
پدیده هایی مانند تاخوردگی پروتئین و واکنشهای اکسیداسیون و احیاء میتوکندری نتیجه فرآیند خودساماندهی است.پدیدۀ خودساماندهی همچنین در تمایز در جنین نیز دیده می شود. در مراحل اولیه تکامل جنینی سلولها در کنار یکدیگر آرامش پیدا می کنند تا جنس اولیه جنینی را بوجود آورند. این مهاجرت و حرکت سلولی ناشی از فرآیند خودساماندهی بوده و منجر به تشکیل الگوی مشخصی می شود.
1.مقدمه
بی تردید استفاده از پدیده های فیزیکی معمول ترین روش در سن سنجی وقایع زمین شناسی بوده و با کمک آن می توان ترتیب بسیاری از اتفاقات زمین شناسی و باستان شناسی را تعیین کرد. در بسیاری از مطالعات، سن و گذشته تاریخی نمونه های یافته شده را با استفاده از قرائن تاریخی موجود مانند نوع پادشاهی حاکم و غیره مشخص میکنند. پر واضح است که این روشها محدودیت و خطاهای فراوانی دارد و از این رو در باستان شناسی مدرن از تکنیکهای سن سنجی قطعی تر و مستقل تری استفاه می شود که از آن جمله می توان به سن سنجی با کربن 14 و پرتوزایی طبیعی نمونه اشاره کرد. در کنار این تکنیکها روش و تکنیک دیگری وجود دارد که نوپا است و بر خلاف سایر روشها اساس شیمیایی داشته و سن سنجی با اسید های آمینه (AAR) نام دارد. دقت در تعیین سن و قابلیت استفاده در علوم مختلف از جمله برتریهای این تکنیک نسبت به تکنیکهای مشابه است و بزرگترین نقطه ضعف آن فراهم کردن اطلاعات در حد مولکولی است و نمی تواند مانند سن سنجی با رادیو کربن در سطح اتمی اطلاعاتی را فراهم کند.
اسید های آمینه مولکولهای آلی کوچکی هستند که پروتئینها را می سازند. اگرچه تعداد زیادی اسید آمینه در طبیعت وجود دارد اما تنها در حدود 20 نوع از آنها در ساختمان پروتئینها بکار می روند. این واحدهای ساختاری زنجیر وار در کنار یکدیگر قرار می گیرند و توسط پیوندی به نام پیوند پپتیدی به یکدیگر متصل می شوند و به این ترتیب یک مولکول پروتئینی را می سازند. از لحاظ ساختاری هر اسید آمینه دارای یک اتم هیدروژن (H)، گروه آمین (NH2)، گروه کربوکسیل (COOH) و یک زنجیره جانبی (R) است که همگی به یک اتم کربن (کربن آلفا) متصل اند. در همه اسید های آمینه به جز گلیسین ریشه R ممکن است یک زنجیره کربنی و یا یک حلقه کربنی باشد. به جز اسید آمینه گلیسین که در آن زنجیره جانبی یک هیدروژن است، در بقیه اسید های آمینه کربن آلفا یک کربن نامتقارن است به این معنی که به چهار مولکول مختلف متصل می باشد. چنین مولکولی کایرال نامیده می شوند. مطابق قرار داد اگر در ساختمان فضایی یک اسید آمینه عامل NH2 متصل به کربن آلفا در طرف چپ باشد، اسید آمینه نوع L و هرگاه در طرف راست کربن آلفا قرار گیرد اسید آمینه از نوع D است
دو ساختار D و L تصویر ایینه ای (اناتیومر یا کایرال) یکدیگرند. مولکولهای کایرال یک اسید آمینه از لحاظ شیمیایی مشابه اند اما در مقابل نور قطبیده رفتار متفاوتی دارند. اسید آمینه L نور قطبیده را به صورت چپ گرد و اسید آمینه نوع D نور قطبیده را به صورت راستگرد می چرخاند. . اسیدهای آمینه طبیعی همگی از نوع L هستند. مجموعه آنزیمی موجود در سلول طی فرایند برگشت پذیر راسمیزاسیون دائما انواع D را به L تبدیل می کند. وقتی موجود زنده ای می میرد کنترل بر روی پیکربندی اسید های آمینه متوقف شده و اسیدهای آمینه نوع L به آرامی به نوع D تبدیل می شوند و مجددا به حالت اول باز می گردند . به این ترتیب در نتیجه مرگ موجود زنده مقدار D تدریجا افزایش یافته و نسبت اسید ها آمینه D به L از صفر به سمت 1 حرکت می کند. با اندازه گیری نسبت D به L اسید های آمینه نمونه می توان زمان مرگ نمونه را تخمین زد. همه اسید های آمینه برای این منظور مناسب نیستند. برای مثال اسید آمینه گلیسین کایرال نیست و یا آلانین در نتیجه واکنشهای تجزیه ای در فسیل تولید می شود [1]. اسیدهای آمینه ای مانند سرین و ترئونین از نظر ترمودینامیکی ناپایدارند و طبیعتا نیمه عمر کمی دارند. به این ترتیب اسیدهای آمینه ای با سرعت راسمیزاسیون مناسب مانند ایزولوسین، لوسین، والین و گلوتامیک اسید و آسپارتیک اسید در مطالعات دیرین شناسی و سن سنجی مورد توجه اند [2].
روشهای شیمیایی سن سنجی از این جهت با تکنیک مبتنی با رادیواکتیو متفاوتند که تکنیکهای شیمیایی تحت تاثیر پارامترهای شیمیایی و محیطی قرار می گیرد. به عبارت دیگر سرعتی که در آن پروتئینها تجزیه شده و یا در اسید های آمینه آن راسمیزاسیون رخ می هد اساسا به ویژگیهای شیمیایی اسید آمینه، موقعیت قرار گیری اسید آمینه در پروتئین، دما و فاکتورهای محیطی محل دفن نمونه (pH، رطوبت ، مقدار کاتیون و آنیون و محتوی می محیط) وابسته است [3]. در زیر برخی از مهمترین عوامل موثر بر راسمیزاسیون اسیدهای آمینه آورده شده است.
2.عوامل موثر بر AAR
AAR شدیدا به دما حساس است [4]. بطوریکه سرعت واکنش برای هر چهار درجه افزایش دما دو برابر می شود. تصویر 2 اثر افزایش دما بر میزان راسمیزاسیون اسید آمینه ایزولوسین را در فسیل نرمتنان مدیترانه تا شمال اروپا نشان می دهد [4]. بعلاوه دمای موثر بر فرایند راسمیزاسیون تحت تاثیر کلیه دماهایی است که بر نمونه از زمان مرگ تا لحظه مطالعه اعمال شده است. برای فسیلی که نیمی از عمر خود را در دمای 0 درجه و نیمه دیگر را در 20 درجه سانتیگراد طی می کند و متوسط دمای محیط این فسیل 10 درجه سانتیگراد است میزان راسمیزاسیون مشابه با نمونه ای است که درکل مدت عمر در 7/16 بوده است [4]. به همین دلیل دما را به صورت دمای موثر در نظر می گیرند. دمای موثر (Teff) مقدار دمایی است که بتواند مقدار راسمیزاسیون محاسبه شده را ایجاد کند. برای نقاطی که نوسانات دمایی روزانه و فصلی آنها زیاد است، مقدار این پارامتر معمولا بیشتر از متوسط دمای اعمال شده بر سیستم است.
مقدار pH سیستم عمیقاً بر راسمیزاسیون اسید های آمینه موثر است. مواد معدنی بیولوژیکی که در محلولهای با pH بالاتر از 9 حرارت دهی میشوند سریعتر از نمونه مشابه ولی در pH طبیعی راسمیزه می شوند [5]. برای مثال مقدار D/L اسید آسپارتیک در صدف نرمتنان با pH 10 ، 29% بیشتر از pH 7 است. میزان حذف اسیدهای آمینه از نمونه نیز با افزایش pH افزایش می یابد [6]. این یافته ها بر این حقیقت تاکید دارد که از این روش نمی توان برای سن سنجی نمونه های به شدت بازی استفاده کرد.
بین وزن مولکولی زنجیره پلی پپتیدی و میزان راسمیزاسیون اسید های آمینه آن رابطه معی برقرار است و این رابطه بیشتر به محل قرارگیری اسید آمینه در زنجیره مربوط است تا وزن مولکولی زنجیره. برای مثال میزان راسمیزاسیون ایزولوسین در قطعاتی با وزنهای کم مولکولی همواره بیشتر از یک قطعه با وزن مولکولی بالا است [7] .
انتقال فیزیکی اسیدهای آمینه به بیرون از بافت نمونه توسط یک فاز مایع ( معمولا آب) شستشو[1] نامیده می شود. سرعت شستشو توسط اندازه مولکول متحرک ، میزان چسبندگی آن به ماتریکس فسیل و قطر مسیر شستشو تعیین می شود [8]. مولکولهایی مانند اسید های آمینه آزاد و پپتیدهای کوچکی که در مسیر قرار دارند ( مولکولهایی با وزن مولکولی کم) نسبت به شستشو حساس اند. با توجه به اینکه اسیدهای آمینه ازاد سرعت راسمیزاسیون بالاتری دارند، شستشو سطح کلی راسمیزاسیون نمونه را کاهش می دهد. در مقابل اسیدهای آمینه ای که به صورت درون کریستالی در ساختار فسیلهای کربناتی شرکت می کنند نسبت به شستشو مقاومند. در حقیقت درون یک کریستال مانند یک سیستم بسته عمل کرده و اسید آمینه را از تغییرات محیطی حفظ می کند. ایزوله بودن درون کریستالها این امکان را فراهم می کند که با اعتبار بالایی از اسیدهای آمینه موجود در آنها برای سن سنجی نمونه استفاده شود [9و3].
3. کاربردها
الف) تعیین سن انسان
اسیدهای آمینه موجود در بافتهای زنده همگی از نوع L هستند و با مرگ موجود ارام ارام به نوع D تبدیل می شوند. تشکیل ساختار D اسیدهای آمینه در بخشهایی با متابولیسم ارام مانند استخوان، دندان، عدسی چشم و مغز ، شاخصی از زمان مرگ می تواند باشد [10و 11]. با استفاده از اندازه گیری نسبت D/L اسید اسپارتیک در پروتئینهای موجود در مینای دندان می توان زمان مرگ یک انسان را تعیین کرد چراکه پروتئینهای موجود در مینای دندان کمتر تحت تاثیر شرایط محیطی قرار می گیرند. معمولا در این تکنیک از GC یا کرماتوگرافی گازی استفاده می شود با اینحال روشهایی مانند HPLC و اسپکتروسکوپی فلورسانس نیز در این نوع از مطالعات دقت بالایی داشته و نتایج درستی فراهم می کنند. لازم به ذکر است که قابل اعتماد بودن نتایج این روش سن سنجی به نوع نمونه گیری، نگهداری و انالیز نمونه ها و داده ها بستگی دارد [12]. فاکتورهای متعددی می تواند راسمیزاسیون آسپارتیک اسید را تحت تاثیر قرار دهد که از آن جمله می توان به نوع دندان، محل نمونه برداری، و آنالیز پروتئینی نمونه اشاره کرد. روش سن سنجی انسان با استفاده ار راسمیزاسیون اسید های آمینه روشی سریع و قابل اعتماد است و تنها نیاز به استفاده از گرافهای کالیبراسیونی دارد که از گروههای مختلف سنی و با دوره های مختلف زمانی تهیه شده باشد [13].
استفاده از AAR در سن سنجی استخوان دارای محدودیتهایی است چراکه شرایط محیطی مانند دما و میزان رطوبت می تواند بر سرعت راسمیزاسیون اسید های آمینه موثر باشد. امروزه از این روش با دقت بسیاری برای تعیین سن استخوان استفاده می شود و این روش اطلاعات خوبی را در ژئوشیمی استخوان، دندان و پروتئینها فراهم می کند. بیشتر مطالعات بر روی استخوان در دمای بالا و وماً در یک سیستم بسته رخ می دهد اما استخوانهای باستانی در یک سیستم باز قرار دارند. ماتریکس استخوان منفذ دار است و بنابراین اسیدهای آمینه می توانند از آن خارج شوند و آلودگیها به آن اضافه گردند. برخی محققان بر این باورند که اگر استخوان در شرایط مناسبی حفظ شده باشد( با دانستن تاریخچه دما و شرایط آب و هوایی) می توان از آن برای سن سنجی استفاده کرد. در بسیاری از تحقیقات از درشت مولکولهای استخوانی مانند کلاژن برای سن سنجی استفاده می کنند [14]. لازم به ذکر است که این روش نیزدارای محدودیتهایی است چراکه کلاژن دارای ساختار سوم پیچیده بوده و در نتیجه چندان به راسمیزاسیون حساس نیست.
ب) تعیین سن نمونه های باستانی
مطالعات نشان داده اند که در صورتی که نمونه مورد مطالعه در مجاورت واکنشهای متابولیسمی قرار نگرفته باشد میزان اسید های آمینه بدون تغییر بوده و ارزش بیشتری برای مطالعات باستان شناسی دارد [11]. یکی از بهترین محیطهایی که در آن پروتئینها و اسید های آمینه حفظ شده باقی می مانند، اسکلتهای کربناتی بی مهرگانی مانند نرم تنان و یا بازوپایان است. مواد آلی به این اسکلتهای کربناتی اضافه شده که یا در میان بلورهای معدنی[2] آن قرار می گیرند و در شکل گیری صدف دخالت میکنند و یا اینکه به صورت درون کریستالی[3] قرار گرفته و انعطاف پذیری صدفها را موجب می شوند [11]. تقریبا تمامی مولکولهای پروتئینی که وارد این ساختارهای کریستالی می شوند از نوع L اسید های آمینه هستند. از لحظه ورود این اسید های آمینه به بافت کربناتی ساعت زمین شناسی آن نیز فعال می شود. ارزیابی سایر نمونهای مطالعاتی مانند اسکلت ماهیها، چوب، استخوان، دندان و مرجانها نیز با این روش ممکن است [15]. همانطور که گفته شد عوامل محیطی مانند دما و میزان رطوبت و نیز مقدار اسید آمینه نمونه می تواند بر کارایی این تکنیک موثر باشد. اپیمریزاسیون ایزولوسین و راسمیزاسیون آسپارتیک اسید معمول ترین اسید های آمینه ای هستند که برای این منظور بکار می روند. برای مثال اسید آمینه آسپارتیک اسید دارای سرعت راسمیزاسیون بالایی است به این خاطر معمولا برای مطالعه نمونه های جوان و یا استخراج شده از مناطق به شدت سرد بکار می رود. اپیمریزاسیون ایزولوسین به آرامی صورت می گیرد و به همین دلیل بیشتر برای سن سنجی نمونه هایی با سن بیشتر از 20000 تا 200000 سال و دمای 24- درجه سانتیگراد مناسب اند [16]. در محیطهایی که دما از این مقدار کمتر باشد از ایزولوسین برای سن سنجی نمونه های قدیمی تر نیز می توان استفاده کرد. اما راسمیزاسیون آسپارتیک اسید سریع است و بیشتر برای مطالعه نمونه هایی با سن تقریبی چند هزار سال تا حد اکثر 80000 سال مناسب است.Goodfriend و همکارانش در سال 1992 در یافتند که این اسید آمینه برای نمونه های 300 ساله نیز کاربرد دارد. در این حالت باید این تکنیک در کنار سایر تکنیکهای سن سنجی استفاده شود [17].
ج) تشخیص بیماریها و اختلالات
تکنیک سن سنجی نه تنها در تعیین سن نمونه های غیر زنده که در تاریخ گذاری و بررسی پیشینه نمونه های زنده و سابقه بیماری در انها نیز کاربرد دارد. مطالعات نشان داده اند که مطالعه بیوشیمیایی راسمیزاسیون اسیدهای آمینه در بیماریهای ماهیچه ای – اسکلتی از اهمیت بسزایی دارد و بوسیله آن می توان زمان آغاز بیماری را سنجید [14]. غلظت اسیدهای آمینه D موجود در بافتها و اندامها در بیماریهای مختلف فرق می کندبرای مثال مطالعات chervyakov و همکارانش نشان دهنده نقش مهم اسیدهای آمینه D در فرایند پیری و ایجاد بیماریهای مغزی مانند اایمر دارد []. همچنین D-اسپارتیل در بسیاری از بیماریهای مرتبط با کهولت سن شناسایی شده است. در جدول 1 برخی از بیماریهای مرتبط با اسیدهای آمینه D اورده شده است. بطور کلی امروزه مطالعه کمی و مقایسه ای اشکال D و L اسید اسپارتیک یک شاخص قدرتمند و قابل اعتماد در تشخیص بیماریهایی نظیر اایمر و آب مروارید است [19].
جدول1. تنوع اسیدهای آمینه D در بیماریهای وابسته به سن []
D- اسید آمینه | منبع | بیماری |
الانین | اایمر | مغز مایع مغزی نخاعی |
اسپارژین | ||
سرین |
پارکینسون شیزوفرنی | مغز پلاسما سرم مایع مغزی نخاعی |
الانین | ||
اسپارتیک اسید | ||
پرولین | ||
سرین |
4. نتیجه گیری
شکل گیری اسیدهای آمینه نوع D در ارگانیزمها و بافتها شاخصی مفید در مطالعه و بررسی تغییرات، بیماریها و اختلالاتی است که در یک بافت رخ می دهد. امروزه از اندازه گیری مقدار تبدیل فرم L به D اسیدهای آمینه در باستان شناسی، پزشکی و پزشکی قانونی استفاده می شود. با کمک AAR به سادگی می توان سن نمونهای زمین شناسی و باستانی را تشخیص داد و بعلاوه با کمک گرافهای کالیبراسیون ، شرایط اب و هوایی حاکم بر زمان مرگ نمونه ها را نیز مشخص کرد. بعلاوه این تکنیک اطلاعات ارزشمندی را برای محققان و کاراگاهان در کشف جنایات فراهم کرده و به افزایش دقت در تشخیص مجرمان کمک می کند. روش انجام ازمایشها معمولا با کمک ابزارهای کروماتوگرافی صورت میگیرد. بدیهی است که پیشرفت تکنیکهای کروماتوگرافی می تواند دقت داده های سن سنجی با اسیدهای آمینه را افزایش دهد.
5. منابع
[1] Devièsea, T., Karavani, I., Comeskeya, D., Kubiaka, C., Korlevi, P. Direct dating of Neanderthal remains from the site of Vindija Cave and implications for the Middle to Upper Paleolithic transition, PNAS, 2017, pp. 1-6.
[2] Hassan, Q., Rakha, A., Bashir, M.Z . Aspartic Acid Racemization with Correlation to Age: A Forensic Perspective, Journal of the College of Physicians and Surgeons Pakistan, 2017, (5),pp. 283-287
[3] Penkman, K.E.H ., Precee, R.C., Keen, D.H.,Collins, M.J . Amino acid geochronology of the type Cromerian of West Runton, Norfolk, UK. Quaternary International ,2010, pp.228:25-37
[4] Miller GH, Hart CP, Roark EB And, and Johnson BJ. Isoleucine Epimerization in Eggshells of the Flightless Australian Birds, Genyornis and Dromaius. In: Goodfriend GA, Collins MJ, Fogel ML, Macko SA, and Wehmiller JF (eds.) Perspectives in Amino Acid and Protein Geochemistry, New York: Oxford University Press.2000.
[5] Bright J and Kaufman DS . Amino acids in lacustrine ostracodes, part III: Effects of pH and taxonomy on racemization and leaching. Quat.Geochronol6, 2011a, pp. 574–597.
[6] Orem C.A., Kaufman D.S. Effects of basic pH on amino acid racemization and leaching in mollusk shell. Quat.Geochronol 2011, pp. 233–245.
[7] Rebeccah A., Warma ck, Clarke G. Racemized and Isomerized Proteins in Aging Rat Teeth and Eye Lens, REJUVENATION RESEARCH Volume 19, Number , 2016, pp. 309-317.
[8] Garde E., Frie A., Dunshea G., Hansen S., Harp seal ageing techniques—teeth, aspartic acid racemization, and telomere sequence analysis, Journal of Mammalogy ,2010, pp.1365-1374.
[9] Bright J ., Kaufman D.S Amino acid racemization in lacustrine ostracodes, part I: Effect of oxidizing pre-treatments on amino acid composition. Quate.Geochronol , 2011b,pp. 154–173.
[11] Klumb K, Matzenauer C, Reckert A, Lehmann K, Ritz-Timme S. Age estimation based on aspartic acid racemization in human sclera., Int J Legal Med. 2016,130(1).pp.207-11.
[12] Dobberstein, R.C,. Huppertz, J., vonWurmb-Schwark, N., Ritz-Timme, S. Degradation of biomolecules in artificially and naturally aged teeth: Implications for age estimation based on aspartic acid racemization and DNA analysis. Forensic Sci. Int. 2008, 179. pp. 1–191.
[13] Kumar, K.Dental age estimation using amino acid racemization, Indian journal of dental research,2008,19 pp. 172-174
[14] Kalíková, K., lechtová, T., Tesaˇrová, E. Enantiomeric Ratio of Amino Acids as a Tool for Determination of Aging and Disease Diagnostics by Chromatographic Measurement , Separations, 2016, 3pp.30- 35.
[15] Kosnik M.A.,Kaufman D.S .Identifying outliers and assessing the accuracy of amino acid racemization measurements for geochronology: II. Data screening. Quaternary Geochronol, 2008, 3(4).pp. 328–341.
[16] Dietl G,P.,Flessa K,W.Conservation paleobiology: Putting the dead to work. Trends in Ecol. Evol, 2011, 26.pp. 30–37.
[17] Goodfriend . Rapid racemization of aspartic acid in mollusc shells and potential for dating over recent centuries. Nature, 1992, 357.pp.399–401.
[] Chervyakov, A.V., Gulyaeva, N.V., Zakharova, M.N. D-amino acids in normal ageing and pathogenesis of neurodegenerative diseases. Neurochem. J. 2011, 5.pp.100–114.
[19] Fujii, N., Takata, T., Fujii, N., Aki, K. Isomerization of aspartyl residues in crystallins and its influence upon cataract. Biochim. Biophys. Ac
[1] Leaching
[2] Intercrystalline
[3] Intracrystalline
گوگل یک موتور جستجوي عمومی است که بوسیله آن می تواند هر مطلبی اعم از عمومی یا تخصصی را مورد
تحقیق قرار دهید با اینحال براي جستجوي مطالب مطالب و مقالات علمی کاملا تخصصی نیز مورد استفاده قرار
می گیرد. براي این منظور باید موارد زیر را در نظر داشت:
- کلمات کلیدي. کلمات کلیدي کلماتی هستند که از دل تحقیق مورد نظر شما خارج می شوند و به شما
کمک می کنند تا محدوده تحقیقاتی گوگل را محدود به مطلب مورد علاقه خود کنید. براي یافتند این
کلمات باید چندین کلمه را امتحان کنید تا به نتیجه مطلوب برسید.
- معمولا در اولین مراحل تحقیق گوگل به شما ویکی پدیا را پیشنهاد می دهد. اگر چه این سایت اطلاعات
مفیدي دارد اما از نظر علمی و اکادمیک قابل استناد نیست اما با کمک مطالب آن می توانید نه تنها
اطلاعات پایه بدست آورید که کلمات کلیدي مناسب تحقیق خود را نیز پیدا کنید.
- اگر تحقیق شما در محدوده جغرافیایی مشخصی است حتما آن را در کلمات کلیدي مورد استفاده مطرح
کنید
- یکی از مشکلات دانشجویان یافتن مقالات رایگان است. براي این منظور می توانید از کلمه pdfدر ادامه
عبارت جستجو استفاده کنید براي مثال Insulin+pdfمی توان شما را به سمت مقالات مرتبط به
انسولین هدایت کند.
- در مراحل ابتدایی تحقیق و یا براي تحقیقهاي کلاسی می توانید از مقالاتی استفاده کنید که شامل جمع
آوري مطالب از مقالات مختلف اند . براي یا فتند چنین کلماتی از عبارت reviewاستفاده کنید. براي
مثال insulin+reviewمقالات مروري مرتبط با انسولین را به شما می دهد.
- ترکیب دو عبارت pdfو reviewاغلب مقالات مروري و معتبر علمی را در رابطه با موضوع مورد تحقیق
شما فراهم می کند.
- اگر براي تحقیق خود به پاورپوینت نیاز دارید می توانید از عبارت pptپس از کلمه کلیدي استفاده کنید
درباره این سایت